メタノールを効率よくエネルギー変換する酵素の立体構造を解明
国立大学法人東海国立大学機構岐阜大学
更新日時:4月30日 14時00分
2026年4月30日
国立大学法人筑波大学
東海国立大学機構岐阜大学
理化学研究所
国立大学法人東北大学
メタノールを効率よくエネルギー変換する酵素の立体構造を解明
メタノールをエネルギー源として利用する酵母において重要な役割を担う酵素の立体構造を、クライオ電子顕微鏡を用いて高精度で解明しました。その結果、よく似た構造の2種類の酵素が環境に応じて異なる働きをする仕組みが明らかとなりました。
カーボンニュートラル社会の実現に向けて、メタノールの効率的な資源化が注目されています。本研究では、より効率的なメタノール利用の鍵を探るため、メタノールで成長する酵母 Ogataea methanolica におけるアルコールオキシダーゼ(AOD)という酵素に着目し、その構造と機能の違いをクライオ電子顕微鏡を用いて明らかにしました。AODには複数の種類があり、細胞のエネルギー代謝の出発点となる、メタノールをホルムアルデヒドへと変換する反応においては、それぞれ異なる働きをすることで円滑なメタノール代謝を実現していることが知られていましたが、そのような性質の違いが生じる理由はこれまで明らかではありませんでした。
本研究では、各AODの立体構造を詳細に比較しました。その結果、全体の構造は類似しているものの、酵素の働きを助ける補酵素の結合様式や、周囲のアミノ酸配置に違いがあることが分かりました。これらの違いが酵素の安定性や電子伝達効率に影響し、結果として酵素活性の差異を生み出している可能性が示唆されました。さらに、タンパク質外周の構造の違いが、酵素活性の安定化に関与していることも明らかになりました。これらの知見から、わずかな構造差が酵素機能に大きな影響を与えることが示されました。この成果は、酵素の分子機構の理解を深めるとともに、高効率な酵素設計や、微生物や酵素を利用したバイオプロセス開発につながると期待されます。
研究代表者
筑波大学 計算科学研究センター
谷 一寿 教授
岐阜大学 応用生物科学部
中川 智行 教授
理化学研究所 放射光科学研究センター/東北大学 多元物質科学研究所
米倉 功治 グループディレクター/教授
研究の背景
近年、地球温暖化対策や資源循環の観点から、カーボンニュートラル社会の実現が求められています。その中で、二酸化炭素やメタンから合成可能なメタノールは、液体で扱いやすく、さまざまな化学製品の原料にもなることから、環境負荷の低い再生可能な炭素資源として重要な物質です。このメタノールを工業的に効率よく利用する手段として、メタノールのみを栄養源として増殖するメチロトローフ酵母 Ogataea methanolica 注1)が広く用いられています。
この酵母は、メタノール分解に関わるアルコールオキシダーゼ(AOD)注2)という酵素を持っています。これには複数の種類があり、特に、低濃度のメタノール環境で効率よく働くMod1pと高濃度環境でも機能するMod2pという2種類のよく似た構造の酵素を使い分けています。しかしながら、両者はアミノ酸配列が約85%も共通しており、なぜこのような働きの違いが生じるのかは長年の課題でした。そこで本研究では、クライオ電子顕微鏡注3)を用いて、Mod1pとMod2pそれぞれの詳細な構造解析を行いました。
研究内容と成果
本研究では、クライオ電子顕微鏡を用いて、両酵素の立体構造を詳細に解析しました(図1)。その結果、いずれも8つのタンパク質からなる安定した構造を形成し、基本的な構造はよく似ていることが分かりました。一方で、機能に関わる重要な違いも明らかになりました。第一に、補酵素FAD注4)の酵素への結合様式が異なり、Mod1pでは通常のFADの一部が変換されたa-FAD注4)が利用されていました。第二に、酵素表面の電荷分布に違いがあり、分子間相互作用や安定性に影響していることが示されました。第三に、タンパク質外周においてアミノ酸配列が大きく異なる領域が存在し(図2)、それに伴い立体構造にも違いが認められ、この差が酵素活性の安定性に関与している可能性が示唆されました。このような構造上の違いが、メタノールに対する反応性や環境適応の差異を生み出していると考えられます。
さらに、これら2種類の酵素が混在した複合体を形成する可能性も示されたことから、環境変化に応じて代謝を柔軟に調節する仕組みがあると考えられます。
本研究により、類似した酵素であっても、わずかな構造の違いが酵素機能の大きな差を生むことが分子レベルで初めて明らかになりました。
今後の展開
本研究成果は、これまで経験的に知られていた酵素機能の違いを、分子レベルで説明するものです。この知見を基に、今後、酵素機能の改良およびバイオ生産技術の高度化を推進し、メチロトローフ酵母を用いた燃料や化学製品の効率的な生産への貢献を目指します。これらの取り組みは、メタノールを原料とするバイオリファイナリー注5)の実現に向けた重要な基盤技術となると期待されます。
参考図
【画像:https://kyodonewsprwire.jp/img/202604308404-O5-Z63a54vB】
図1 Mod1pおよびMod2pの立体構造比較。(a)全体構造。両構造は非常によく類似している。各モノマーは異なる色で示している。 (b) Mod1p(緑)およびMod2p(黄)のモノマー構造の重ね合わせ。(c) Mod1pおよびMod2pのFAD結合部位の比較。Mod1pのa-FADにおけるC2′-OH基(左図赤矢頭)は観察者側を向いているのに対し、Mod2pの標準的なFADにおけるC2′-OH基(右図オレンジ矢頭)は観察者と反対方向を向いている。FADと相互作用する酵素のアミノ酸残基を棒モデルで表示するとともに各残基の名称と番号を示す。点線は水素結合を示す。
【画像:https://kyodonewsprwire.jp/img/202604308404-O6-KZs2eP40】
図2 Mod1pとMod2pの間でアミノ酸配列が大きく異なる領域。最も配列差の大きい領域を赤色(a, b)またはオレンジ色(c)で示す。(b, c) 相互作用しているアミノ酸残基を棒モデルで表示する。*は隣接するアミノ酸分子を示す。
用語解説
注1) メチロトローフ酵母 Ogataea methanolica
メタノールなどの炭素数が1つの化合物(C1化合物)を唯一の炭素源およびエネルギー源として利用し、増殖できる酵母。工業用酵素や医薬品の製造に広く利用されている。
注2) アルコールオキシダーゼ(AOD)
アルコールを酸化してアルデヒドと過酸化水素を生成する酵素。特にメタノールを基質として酸化する性質を持ち、主に微生物におけるメタノール代謝において重要な役割を果たしている。
注3) クライオ電子顕微鏡
生体高分子の立体構造を解析する手法の一つ。タンパク質などの試料を急速凍結して観察することで、結晶化することなく、アミノ酸や原子の位置を明らかにできる。
注4) 補酵素FAD(flavin adenine dinucleotide)
リボフラビン(ビタミンB₂)から誘導される、細胞のエネルギー代謝における酸化還元反応に必須の補酵素。細胞内でATP産生を支える役割を担っている。メチロトローフ酵母においては、通常のFADに含まれる糖アルコールのリビトール鎖がアラビトール鎖へと置き換わった特殊なFAD(arabityl FAD, a-FAD)が存在し、これが結合したAODは最大反応速度がわずかに低下するものの、低メタノール濃度環境に適応した反応が可能となる。
注5) バイオリファイナリー
化石資源に依存せず、植物などに由来する再生可能資源であるバイオマスを原料として、微生物や酵素の働きにより燃料や化学品を生産する技術およびそれに関連する産業を指す。カーボンニュートラル社会の実現に向けた鍵の一つとして期待されている。
研究資金
本研究は、国立研究開発法人日本医療研究開発機構(AMED)創薬等ライフサイエンス研究支援基盤事業(BINDS)(JP21am0101118、JP22ama121006、JP25ama121004)、JST未来社会創造事業(JPMJMI23G2)、科研費(JP18K19875)、量子情報生命科学研究センター等の助成を受けて実施されました。
掲載論文
【題 名】 Cryo-EM structures of alcohol oxidase isozymes reveal structural determinants of cofactor variation and enzymatic activity in Ogataea methanolica
(Ogataea methanolica由来アルコールオキシダーゼのクライオ電子顕微鏡構造による補酵素の多様性および酵素活性決定機構の解明)
【著者名】 Hao-Liang Cai1, Atsuhiro Shimada1,2,3, Tasuku Hamaguchi4,5, Akira Mizoguchi6,
Koji Yonekura4,5, Kyohei Tsuchiyama2, Masaya Shimada1,2,3,7, Akio Ebihara1,2,3,7, Kazutoshi Tani6,8,9,*, Tomoyuki Nakagawa1,2,3,7,*
1 The United Graduate School of Agricultural Sciences, Gifu University, 1-1 Yanagido, Gifu 501-1193, Japan. 2 The Graduate School of Natural Sciences and Technologies, Gifu University, 1-1 Yanagido, Gifu 501-1193, Japan. 3 Faculty of Applied Biological Sciences, Gifu University, 1-1 Yanagido, Gifu 501-1193, Japan. 4 RIKEN SPring-8 Center, 1-1-1, Kouto, Sayo, Hyogo 679-5148, Japan. 5 Institute of Multidisciplinary Research for Advanced Materials, Tohoku University, 2-1-1 Katahira, Aoba-ku, Sendai 980-8577, Japan. 6 Graduate School of Medicine, Mie University, 2–174 Edobashi Tsu, Mie 514-8507, Japan. 7 Preemptive Food Research Center, Gifu University, 1-1 Yanagido, Gifu, 501-1193, Japan. 8 Center for Computational Sciences, University of Tsukuba, 1-1-1 Tennodai, Tsukuba, Ibaraki 305-8577, Japan. 9 Center for Quantum and Information Life Sciences, University of Tsukuba, 1-1-1 Tennodai, Tsukuba, Ibaraki 305-8577, Japan.
【掲載誌】 Microbial Biotechnology
【掲載日】 2026年4月18日
【DOI】 10.1111/1751-7915.70355
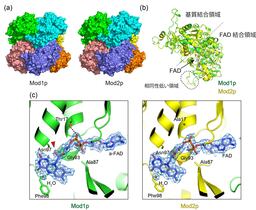
図1
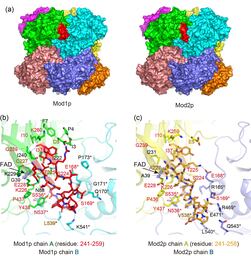
図2

